Chlorination Plant – dalam proses produksi energinya, pembangkit listrik thermal seperti PLTU memerlukan sejumlah air laut dengan kapasitas yang besar dan kualitas yang baik agar dapat digunakan. air laut yang masuk pada proses produksi pembangkit listrik tentunya masih banyak mengandung berbagai mikrooganisme / biota laut yang dapat menghambat sistem transfer panas pada condenser atau pada sistem lainnya seperti balance of plant. Nah untuk mengatasi permasalahan tersebut maka diperlukanlah peralatan yang disebut chlorination plant, bagaimana cara kerjanya, yuk kita simak ulasan singkat berikut ini
baca juga:
Chlorination Plant
Reaksi kimia
 Reaksi kimia dalam Electrolyzer diperlihatkan dengan gambar disamping :
Reaksi kimia dalam Electrolyzer diperlihatkan dengan gambar disamping :
Electrolysis dalam Electrolyzer:
Aliran air laut berada diantara kedua elektrode (anode dan cathode) dalam Electrolyser dihubungkan ke sumber arus DC, reaksi kimia yang terjadi didalam electrolyzer antara chlorine dan caustic soda yang dihasilkan oleh elektrolisis.
Reaksi Chlorinasi:
Arus searah, lewat melalui air laut yang mengalir dalam Electrolyzer, dimana sodium chloride (NaCl) diuraikan menjadi ion Na+ dan Cl-, dengan reaksi kimia sebagai berikut :
Persamaan Reaksi:
2NaCl —-> 2Na+ + 2Cl-
Katoda: 2Na+ + 2e- —-> 2Na
2Na + 2H2O —-> 2NaOH + H2
Anoda: 2Cl- —-> Cl2 + 2e-
Cl2 + 2NaOH —-> NaOCl + NaCl + H2O
2NaCl + 2H2O —-> NaOCl + NaCl + H2O + H2
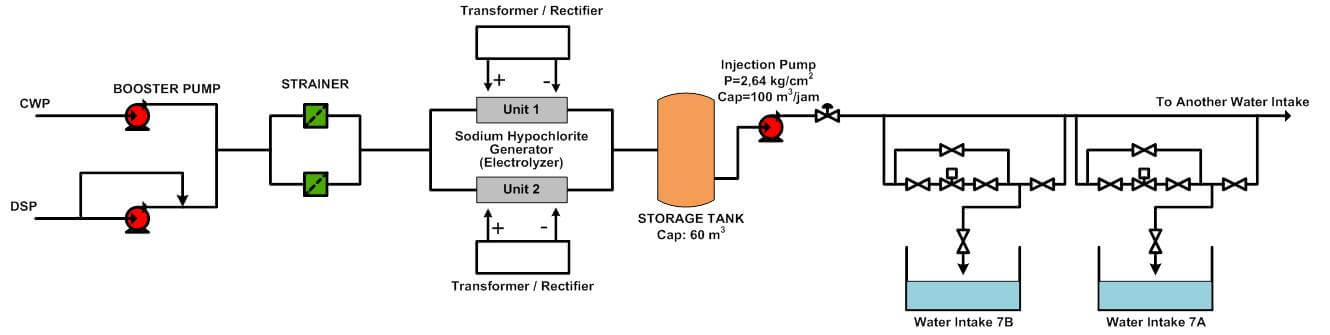
Prinsip kerja Chlorination Plant
Pada suhu dan tekanan normal, senyawa chlorine berbentuk gas. Tetapi dapat diubah dalam bentuk padat ataupun cair. Pada penggunaannya, senyawa chlorine terdiri dari bleaching powder, calcium hypoclorite / NaOCl & sodium hypochlorite dengan teknologi tipe electrical ataupun gas.
Proses pembentukan senyawa calcium hypoclorite / NaOCl menggunakan prinsip elektrolisa air laut. Awal mula air laut yang sudah melewati strainer dipompakan masuk kedalam modul elektroliser yang dialiri arus listrik searah atau DC. Senyawa air laut yang terdiri dari garam dan air tersebut kemudian terurai,
Garam: NaCl menjadi ion NA+ dan ion CL-
Air: H2O menjadi ion 2H+ dan ion O2.
Karena ion 2H+ cenderung lebih stabil jika berdiri sendiri, maka ion 2H+ merubah membentuk molekul gas hydrogen yaitu gas H2 yang kemudian dibuang melalui Degassing / Hypo Tank. Sedangkan ion O2 cenderung lebih negative terhadap ion Na+ dan ion Cl-. Akibatnya ketiga ion tersebut bersatu membentuk ikatan yang lebih stabil yaitu molekul NaOcl / sodium hypochlorite ( klorin ) yang kemudian disimpan dalam storage tank sebelum nantinya diinjeksikan pada air laut sebelum travelling screen.
Elektrolisa untuk memicu reaksi kimia pembentukan sodium hypochlorite pada air laut dapat dapat dijelaskan sebagai berikut :
NaCl ————— Na+ + Cl–
Pada sis Anoda : 2Cl– – 2e ———- Cl2
Pada sisi Katoda : 2Na+ + 2H20 + 2e ————— 2 NaOH + H2
Reaksi Total : 2 NaCl + 2 H2O —————— 2 NaCl + 2 H2
Untuk memastikan operasional chlorine plant efektif dan efisien, maka perlu dilakukan pemantauan terhadap residual chlorine di sisi out fall. Nilai residual chlorine yang dijaga agar instalasi pembangkit terhindar dari biota laut adalah 0,05 – 0,3 ppm
Mode Operasi
Injeksi/dosing sodium hypochlorite pada saluran masuk air laut (seawater intake channel) diatur sebesar 1 ppm
Diatur sebesar 3 ppm selama 20 menit tiga hari sekali. Shock dosing bertujuan mengganggu kekebalan biota laut terhadap dosing sodium hypochlorite sebesar 1 ppm, sehingga diharapkan dengan shock dosing ini biota-biota laut yang telah beradaptasi dengan injeksi NaOCl sebesar 1 ppm dapat dilumpuhkan


Mohon Ijin, apabila ada yg mempunyai relasi untuk penjualan sistem electro chlorination. bisa hubungin wa : 08988198308 Yulia, atau email : [email protected]